水質有害物質特論では1~17章で出題傾向が明確にあります。
出題傾向の記事は下の記事をご参照ください。
1~17章において、ほぼ毎年出題される章があります。
今回解説する3章のシアン排水の処理からもほぼ毎年出題されます。
そこで、本記事で内容を理解し、公式の本で詳細を読み込むことをオススメします。
(※あえて内容を省いているところがあるので、ご注意ください。)
9章の内容紹介
9章の内容はシアン排水の処理方法を説明した章です。
シアン排水の処理方法は金属排水の処理方法とはかなり異なります。
金属排水は金属を沈殿させることで処理していました。
しかし、シアンの場合はシアンを分解することで無害化します。
そのため、「どのようにシアンを分解するか?」という内容に主眼が置かれています。
(分解できないシアンは沈殿させます。)
アルカリ塩素法
シアン(CN)を分解する方法の一つ目はアルカリ塩素法です。
次亜塩素酸NaOClを使用することでシアンを最終的に窒素N2と二酸化炭素CO2にします。
アルカリ塩素法の特徴は二段階で反応を起こすことにあります。
一段階目はアルカリ性pH10以上、二段階目で中性pH7~8で反応を起こします。
反応としては以下のようになります。
一段階目:pH10以上
NaCN + NaOCl → NaCNO + NaCl
二段階目:pH7~8
2NaCNO + 3NaOCl +H2O → N2 + 3NaCl + 2NaHCO3
(NaHCO3 ⇄ NaOH + CO2)
二段階で反応を行う理由は反応速度です。
一段階目で生成されたシアン酸NaCNOの分解がアルカリ性よりも中性の方が速いため、二段階目を中性にして反応を行います。
反応速度は一段階目が約10分、二段階目が約30分程度です。
手順をまとめると以下になります。
- NaOHを添加 :pHを10以上にする
- NaOClを添加 :シアンNaCNをシアン酸NaCNOにする
- H2SO4を添加 :pHを7~8にする
アルカリ塩素法で分解できるものと出来ないもの
アルカリ塩素法で分解できる金属シアン化物と分解できない金属シアン化物があります。
それをご紹介します。
まず、分解できるものは以下です。
- アルカリ金属塩 :NaCN、KCN
- 銅シアノ錯体 :Na3〔Cu(CN)4〕
- 亜鉛シアノ錯体 :Na3〔Zn(CN)4〕
- カドミウムシアノ錯体 :Na3〔Cd(CN)4〕
やや難分解性のもの :過剰塩素と長時間の反応で分解可能
- ニッケルシアノ錯体 :Na3〔Ni(CN)4〕
- 銀シアノ錯体 :Na〔Ag(CN)2〕
次にアルカリ塩素法で分解出来ない金属シアノ化合物をまとめました。
- 鉄シアノ錯体 :Na4〔Fe(CN)6〕
- コバルトシアノ錯体 :Na4〔Co(CN)6〕
- 金シアノ錯体 :Na〔Au(CN)2〕
紺青法(こんじょうほう)(難溶性錯化合物沈殿法)
続いて、分解できない金属シアノ化合物を処理する方法をご紹介します。
方法としては、沈殿させます。
重金属塩を添加すると難溶性塩が生成されるので、凝集沈殿法で処理します。
例として、鉄シアノ化合物の難溶性塩としてFe3〔Fe(CN)6〕2(ターンブルブルー)があります。
このターンブルブルーを生成し、鉄シアノ化合物を除去する方法が紺青法です。
反応式としては以下となります。
2〔Fe(CN)6〕3 + 3Fe2+ → Fe3〔Fe(CN)6〕2 :pH5~6
もしFe2+が少ない場合、可溶性のFe〔Fe(CN)6〕(可溶性プルシアンブルー)が生成され、処理水に着色が残り、不完全な処理になります。
さらに、pHが上がると水酸化鉄と可溶性の鉄シアノ錯体に分解されるため、弱酸のpH5~6にする必要があります。
通常、紺青法はアルカリ塩素法の後に行われます。
図にすると以下のようになります。
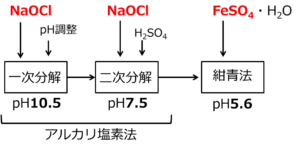
なお,Fe2+の供給源はFeSO4になります。
オゾン酸化法
オゾンを使用したシアンの分解法もあります。
オゾンを使用した場合、シアンは窒素N2と炭酸水素塩HCO3に分解されます。
反応式は以下になります。
CN + O3 → CNO– + O2
2CNO– + 3O3 → 2HCO3 + N2 + 3O2
オゾン酸化法は微量の銅やマンガンが存在すると、触媒効果で分解効率が向上します。
なお、やや難分解性のニッケルシアノ錯体は分解され、酸化ニッケル(III)Ni2O3となります。
ただし、難分解性の鉄Fe、金Au、銀Agの錯体は分解困難です。
電解酸化法
濃厚シアン廃液を処理する場合は、薬剤添加による酸化法では発熱や塩素の揮発などの問題が生じます。
そのため、濃厚廃液の場合は電解酸化法が適しています。
電解酸化法による分解反応は以下です。
CN– + 2OH– → CNO + H2O + 2e–
2CNO– + 4OH– → 2CO2 + N2 + 2H2O + 6e–
CNO– + 2H2O → NH4+ + CO32-
ただし、電解酸化法が適さない場合もあります。
まず一つは、濃度が低い廃液です。
濃度が低い場合電気が流れにくいため、分解効率が悪くなります。
また、鉄やニッケルのシアノ錯体の分解は困難です。
生物分解法
シアンを生物処理する方法もあります。
シアン排水には有機物の共存量が多いため、好気微生物処理の一つである活性汚泥法が適用されます。
この方法は、活性汚泥にシアン排水を少量ずつ添加し、微生物に耐性を持たせシアンを分解、資化する菌を増殖させる方法です。
吸着法
難分解性のシアノ錯体を吸着材で捕捉する処理方法もあります。
鉄シアノ錯体は活性炭に吸着させ、アルカリで遊離させることが出来ます。
酸分解燃焼法
シアンは低いpHではシアン化水素という揮発性の化合物になります。
そのため、pHを酸性にし、曝気すればシアン化水素としてシアンを処理することが出来ます。
pH1以下ではほとんどのシアノ錯体はシアン化水素と金属イオンに分解されます。
発生したシアン化水素ガスは水酸化ナトリウムNaOHに吸収させてシアン化ナトリウムとして回収、または燃焼して二酸化炭素CO2と窒素N2に分解します。
まとめ
この章ではシアン排水の処理方法を説明しています。
基本的にはアルカリ塩素法でシアン化合物を分解し、紺青法で難分解性のシアン化合物を処理します。
アルカリ塩素法のポイントは以下となります。
- 次亜塩素酸NaOClでシアンを分解
- 二段階で分解を行う。一段階目はアルカリ性pH10以上、二段階目は中性pH7~8
- 最終生成物は窒素N2と二酸化炭素CO2
- 分解できないものは鉄、コバルト、金のシアノ錯体
また紺青法のポイントは以下となります。
- 主に鉄シアノ錯体に使用
- Fe2+(=FeSO4)で難溶性塩を生成する
- 弱酸性pH5~6で行う
- 基本的にアルカリ塩素処理後に行われる
アルカリ塩素法および紺青法は頻出なのでしっかり勉強することをオススメします。
また、その他の処理方法は内容を出題されるというよりは、適した処理法はどれかといった内容で出題される傾向にあります。